الخلائط
_1 - الخليط المتجانسالخليط المتجانس هو كل خليط لا يمكن التمييز بين مكوناته بالعين المجردة .متل الماء و الملح - الماء و السكر- الماء و الحليب- البنزين و الزيت .........
2- الخليط غير المتجانسالخليط الغير المتجانس هو كل خليط يمكن التميز بين مكوناته بالعين المجردة مثل الماء و الزيت- الرمل و الماء- التراب و الحجر......
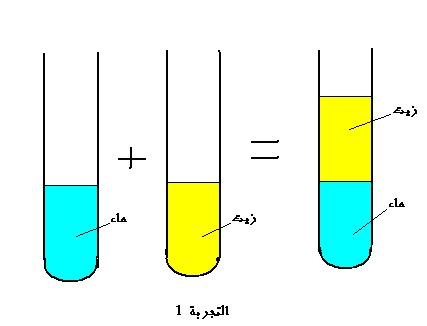
3 - خليط بين سائلين1-تجربة- نخلط كمية من الماء مع كمية من الزيت فنحصل على خليط غير متجانس (التجربة 1).
- نخلط كمية من الماء مع كمية من الكحول في انبوب اختبار فنحصل على خليط متجانس ( التجربة2) .
 استنتاج
استنتاجالحصول على خليط غير متجانس في التجربة (1) يدل علي ان الماء والزيت سائلان غير قابلان للامتزاج
-الحصول على خليط متجانس في التجربة (2) يدل على ان الماء والكحول سائلان قابلان لامتزاج.
3- خليط بين جسم سائل وصلب 1)-تجربةنضيف الى كميات متساويات من الماء كميات مختلفة من الملح فنلاحظ اختفاء الملح في الانبوب(1) و(2) وترسب كمية منه في الانبوب(3)
 2-استنتاج
2-استنتاج- الحصول على خليط متجانس في الانبوب(1) يدل على ان الملح قابل للذوبان في الماء.
- الملح يسمى الجسم المداب والماء يسمى الجسم المذيب.
- الخليط المتجانس المحصل عليه يسمى (محلول الملح) .
3)- تعاريف- المحلول هو خليط متجانس نحصل عليه بإذابة جسم في الماء.
- في الانبوب (1) ملوحة المحلول ضعيفة ادن يسمي محلول مخفف .
- في الانبوب (2) ملوحة المحلول كبيرة و مازال قادرا على إذابة الملح ادن هو محلول مركز .
- في الأنبوب (3) ملوحة المحلول كبيرة و لكنه لم يعد قادرا على إذابة ملح جديد ادن هو محلول مشبع .
-
4- الذوبانية و التركيز الكتلي 1- الذوبانيةالذوبانية هي عدد يميز كل مادة قابلة للذوبان في الماء ونرمز لها ب S و وحدتها g/L . وهي اكبر كمية من جسم يمكن أذابتها في لتر واحد من الماء و نحصل على محلول مشبع .
- والذوبانية تتغير حسب درجة الحرارة بحيث كلما ارتفعت درجة الحرارة ترتفع الذوبانية .
2- أمثلة - ذوبانية الملح في الماء عند درجة الحرارة العادية ( C200) هي S = 360 g/L .
- ذوبانية السكر في الماء في درجة الحرارة العادية ( C200) هي S= 2000g/L .
3 - التركيزالكتلي التركيزالكتلي هو العدد C ويميز كل محلول ووحدته . g/L
و يحسب باستعمال العلاقة التالية
C = M/V .
بحيث M هي كتلة الجسم المداب ب ( g ) .
و V هو حجم الجسم المذيب (الماء) ب ( L) .
2 خاصية قبل تحضير المحلول و بمعرفة الذوبانية S وبحساب التركيزالكتلي فانه :
*إدا كان C < S فإننا نحصل على محلول مخفف أو مركز .
*اذا كان C = S فإننا نحصل على محلول مشبع دون تكون راسب .
* اذا كان C > S فإننا نحصل على محلول مشبع مع تكون راسب.
- تمرين تطبيقي1- نضع kg 2 من الملح في L 5 من الماء .وعلما ان g 360 s= مادا سيحصل ?
2- في حالة تكون راسب احسب كتلته .
3- نضع g 600 من جسم A في L5 من الماء فيذوب جزء منه ويترسب g50 منه احسب ذوبانيته .
4- نضع g200 من هدا الجسم في 0.5L من الماء مادا سيحصل ?
6- خليط بين سائل و غاز يمكن لبعض الغازات ان تذوب في بعض السوائل متل
-المشروبات الغازية تحتوي على الغاز الكربوني الدي يساعد على الهضم .
-ماء البحر يحتوي على الأكسجين مداب فيه والدي تتنفسه الأسماك
7- خليط الغازات جميع الغازات عموما قابلة للامتزاج فيما بينها.
مثلا الهواء خليط من عدة غازات هي
- غاز الأكسجين بنسبة 21% .
- غاز الآزوت بنسبة 78% .
- غازات أخرى بنسبة 1% .
[/size]
